新闻资讯
Activation of hypothalamic-pontine-spinal pathwaypromotes locomotor initiation and functional recoveryafter spinal cord injury in mice
” 的文章。该研究致力于解析下丘脑外侧区(LHA)整合内在动机、并向脊髓传递运动指令的核心机制。

01 研究目的
2025年12月6日,李毅团队在 Nature Communications 杂志上在线发表题为 “Activation of hypothalamic-pontine-spinal pathwaypromotes locomotor initiation and functional recoveryafter spinal cord injury in mice” 的文章。该研究致力于解析下丘脑外侧区(LHA)整合内在动机、并向脊髓传递运动指令的核心机制。通过精准鉴定调控觅食等动机驱动型运动的专属神经环路,研究明确了LHA不同神经元亚型及其下游通路的功能分工。在此基础上,团队进一步探索了LHA相关环路在脊髓损伤(SCI)后的运动修复作用,并研发了靶向LHA的深部脑刺激(DBS)新策略,旨在为SCI患者的运动功能重建开拓全新方向。
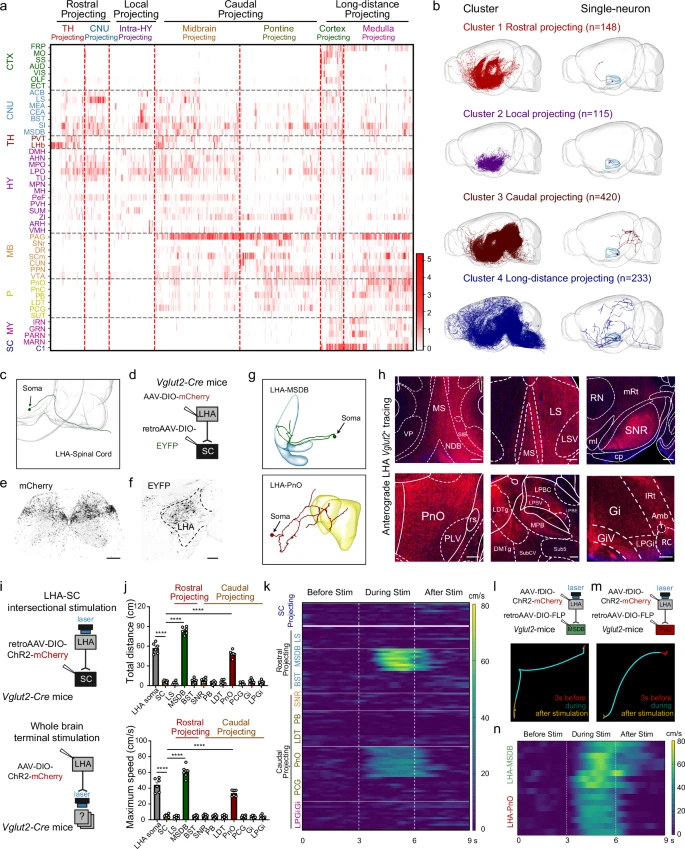
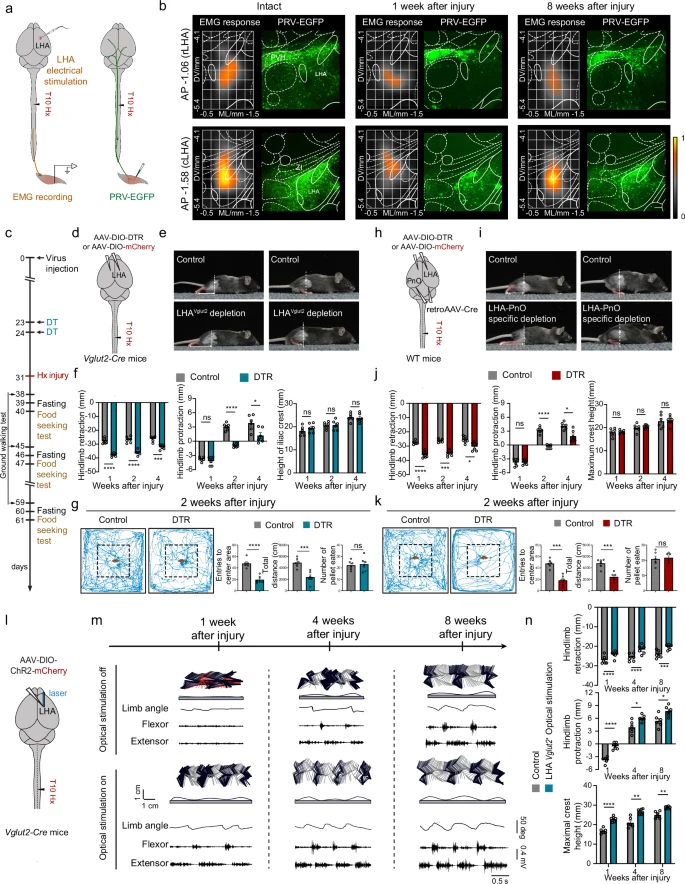
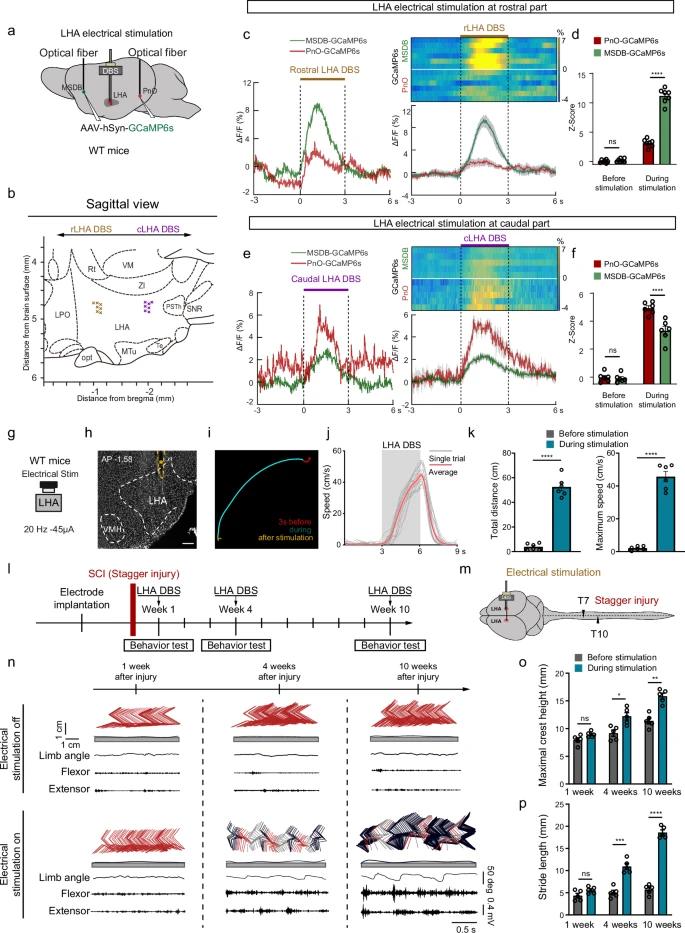
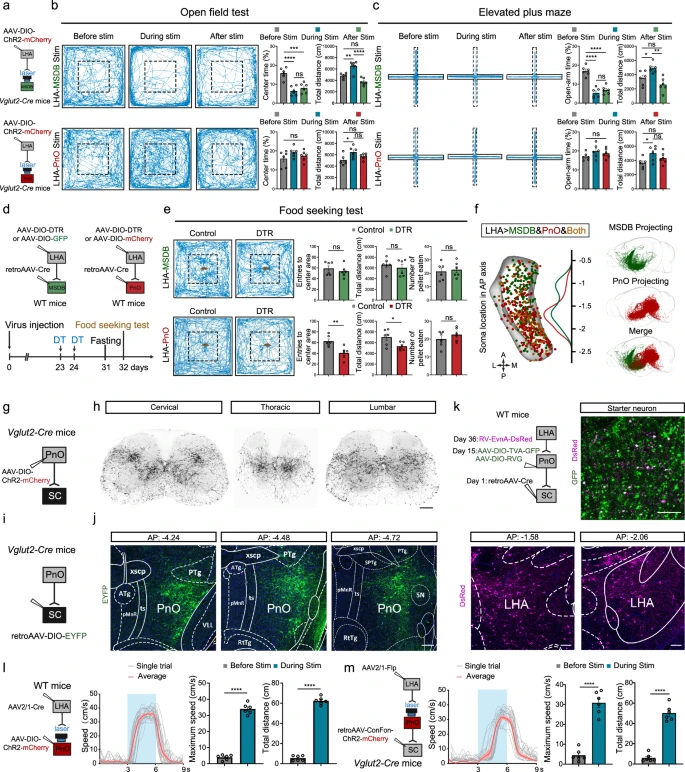
02 研究方法 1 神经示踪技术 逆行跨突触示踪:向小鼠后肢胫骨前肌、腓肠肌注射表达 EGFP 的伪狂犬病毒,标记支配后肢肌肉的上游神经元,结合 ClearMap 技术完成全脑神经元分布分析。 顺行与逆行示踪联用:通过注射特异性 AAV 病毒,追踪下丘脑外侧区与脑桥网状核口部、内侧隔核和斜角带及脊髓间的神经连接通路。 单神经元投射组分析:对下丘脑外侧区神经元开展稀疏标记与全脑成像,依据神经元投射模式进行层级聚类分类。(见图1、2) 图1:下丘脑中的LHA谷氨酸能神经元主要参与后肢运动控制,并对动机驱动的运动至关重要 2 光遗传学与化学遗传学技术 光遗传学激活:在特定基因编辑小鼠的下丘脑外侧区注射靶向 AAV 病毒,通过光纤激光刺激目标神经元或神经末梢,观察小鼠运动行为的动态变化。 化学遗传学抑制:向特定基因编辑小鼠的脑桥脚核注射靶向 AAV 病毒,通过注射 CNO 抑制核团内谷氨酸能神经元,验证下丘脑外侧区 - 脑桥网状核口部通路的功能独立性。(见图1、2) 图2:LHA回路背后的神经回路单神经元投影组引导分析,用于运动控制 3 钙成像与电生理记录 光纤光度法:向下丘脑外侧区注射钙指示剂 AAV 病毒,记录自由活动小鼠在觅食、休息、进食等不同行为状态下,核团内神经元的钙信号变化。 单细胞记录:借助多电极阵列,在小鼠线性轨道行走过程中记录下丘脑外侧区神经元的放电活动,分析神经元放电与运动速度的关联特征。 肌电图记录:在小鼠后肢肌肉植入电极,记录下丘脑外侧区受刺激后,后肢肌肉的收缩反应情况。 图3:LHA-PnO回路的功能重组有助于自发运动恢复 4 动物模型与行为学测试 脊髓损伤模型:构建小鼠单侧脊髓半横断的不完全性损伤模型,以及交替侧半横断的严重脊髓损伤模型。 行为学测试:开展旷场试验、觅食试验、地面行走试验、高架十字迷宫试验,分别评估小鼠基础运动能力与焦虑样行为、动机驱动型运动能力、后肢运动学特征及焦虑水平。(见图1、3、4) 图4:优化后的LHA DBS急性化使慢性错位性脊髓损伤后瘫痪小鼠能够逐步进入 5 基因操作与深部脑刺激技术 神经元消融:通过注射靶向 AAV 病毒结合白喉毒素,实现对下丘脑外侧区谷氨酸能神经元,以及向下脑桥网状核口部投射的下丘脑外侧区神经元的特异性消融。 意向门控深部脑刺激:结合脑机接口技术,通过解码运动皮层神经元的活动信号触发下丘脑外侧区的深部脑刺激,实现对目标核团的精准化刺激调控。 03 研究内容 1 LHA 谷氨酸能神经元调控后肢运动 通过 PRV 示踪发现,LHA 是下丘脑内支配后肢肌肉的神经元密度最高的区域,且这类神经元主要集中在尾侧 LHA。光遗传学技术激活 LHA 的 Vglut2⁺神经元,可诱导小鼠产生强烈的运动行为,且运动强度与光刺激的频率、强度呈相关性;而激活 LHA 的 Vgat⁺神经元则无此运动诱导效应。单细胞记录结果显示,部分 LHA 神经元的放电率与小鼠运动速度呈正相关,这类神经元中多数为谷氨酸能神经元,且有部分神经元在运动起始前放电率已出现升高趋势。(见图1) 2 LHA 通过 PnO/MSDB 通路调控运动 经单神经元投射组分析,可将 LHA 神经元划分为多类及不同亚型,其中尾侧投射型神经元主要向 PnO 等脑桥区域投射,长距离投射型神经元中有部分可直接投射至脊髓。光刺激 LHA 直接投射至脊髓的神经元,无法诱导小鼠产生运动行为;而刺激 LHA 向 PnO 或 MSDB 的投射通路,均可启动小鼠运动,且不同通路触发的运动表现存在差异:MSDB 投射通路会触发小鼠高速逃逸样运动,PnO 投射通路则诱导小鼠产生温和的运动行为。通过化学遗传学抑制 PPN 谷氨酸能神经元后,LHA-PnO 通路仍可正常诱导运动,证实该通路具备功能独立性。(见图2) 3 LHA-PnO 通路特异性调控动机驱动型运动 觅食试验中检测发现,LHA Vglut2⁺神经元在小鼠运动起始时钙信号显著升高,进食过程中则呈降低趋势;而 LHA 内抑制性神经元在小鼠进食时被激活。特异性消融向 PnO 投射的 LHA 神经元后,小鼠在旷场试验中的基础运动能力无明显异常,但在觅食试验中进入区域中心的次数和总移动距离均显著减少,且该操作未对小鼠食欲产生影响。高架十字迷宫与旷场试验结果显示,刺激 LHA-PnO 通路不会引发小鼠的焦虑样行为,而刺激 LHA-MSDB 通路则会导致小鼠出现焦虑相关的行为反应。 图5:LHA-PnO脊髓通路对于将运动信号从下丘脑传递到脊髓至关重要 4 LHA-PnO - 脊髓通路介导 SCI 后运动恢复 脊髓损伤模型构建后,短期观察发现 LHA 神经元的 PRV 标记量显著减少;慢性期时,尾侧 LHA 的标记神经元数量出现恢复,提示 LHA 与脊髓之间的神经连接可在脊髓损伤慢性期完成重建。特异性消融 LHA 谷氨酸能神经元,或向 PnO 投射的 LHA 神经元后,脊髓损伤小鼠的后肢伸展、回缩等运动相关参数均显著受损,同时伴随明显的觅食行为障碍。光遗传学激活 LHA Vglut2⁺神经元,可即时改善脊髓损伤小鼠的后肢运动功能,显著提升其体重支撑能力与步幅长度。(见图3) 5 优化 DBS 策略促进严重 SCI 后的运动恢复 针对 LHA 不同亚区的定位刺激研究发现,刺激尾侧 LHA 可优先激活 PnO,刺激嘴侧 LHA 则优先激活 MSDB,据此选择尾侧 LHA 作为深部脑刺激的靶点,可有效避免刺激引发的焦虑样副作用。对严重脊髓损伤小鼠实施尾侧 LHA 的急性深部脑刺激,干预后中期小鼠后肢运动的相关运动学参数已显著改善,且该改善效应可长期维持。采用结合脑机接口的意向门控长期深部脑刺激策略,通过解码运动皮层神经元活动触发 LHA 深部脑刺激,对严重脊髓损伤小鼠进行长期规律性刺激后,其运动功能评分显著提升,后肢自主运动能力得到有效恢复,且整个刺激过程未引发小鼠明显的应激反应。(见图4) 04 创新点 首次鉴定出下丘脑 - 脑桥 - 脊髓通路(LHA-PnO-SC),明确其为调控动机驱动型运动的核心环路,且独立于经典的中脑运动区(MLR)通路。 发现 LHA 神经元功能分区:cLHA-PnO 通路介导无焦虑的动机性运动,rLHA-MSDB 通路调控逃逸样焦虑相关运动,实现运动与情绪功能的分离。 开发意向门控 DBS 技术,结合 BCI 解码运动皮层意向信号,精准触发 LHA 刺激,既避免了持续 DBS 的副作用,又能长期促进严重 SCI 后的运动功能恢复,为临床转化提供新范式。 05 技术启示 神经环路的特异性是精准治疗的关键:LHA-PnO通路的发现表明,针对特定神经亚型和投射通路的精准调控,可在实现疗效的同时最大限度减少副作用,为神经调控治疗提供了新范式。 脑-脊髓环路重组是功能恢复的基础:本研究证实,上位中枢(如下丘脑)的功能可塑性对SCI恢复至关重要。未来的康复策略需兼顾中枢环路激活与脊髓局部修复。 脑机接口与神经调控的结合潜力巨大:“意向门控”DBS将“患者主动意图”与“精准刺激”相结合,显著提升了治疗的有效性与安全性,为神经损伤后的功能重建开辟了新方向。 从基础到临床的转化路径清晰:通过构建不同严重程度的SCI模型并系统优化刺激参数,本研究为LHA-DBS从动物实验迈向临床应用奠定了坚实基础,有望破解SCI运动功能恢复的临床难题。 参考文献:Ji C, Zhang Y, Lin Z, Zhao Z, Jiao Z, Zheng Z, Shi X, Wang X, Li Z, Yu S, Qu Y, Wei Y, Rui T, Zheng B, Xie T, Shi H, Wang Q, Yu X, Xu X, Chen J, Fan J, Cai W, Li Y. Activation of hypothalamic-pontine-spinal pathway promotes locomotor initiation and functional recovery after spinal cord injury in mice. Nat Commun. 2025 Dec 6;17(1):446. doi: 10.1038/s41467-025-67133-5IF: 15.7 Q1 . PMID: 41353490. 创作声明:本文是在原英文文献基础上进行解读,存在观点偏向性,仅作分享,请参考原文深入学习。 图文编辑 | 赵 玉 图文审核 | 伍金嵘 -END-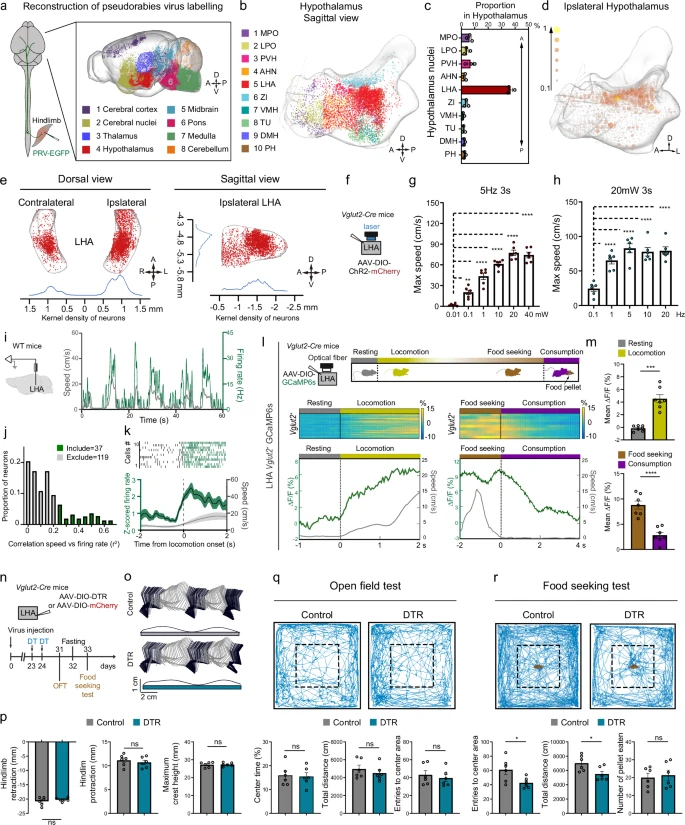



订购和售后

邮箱:consentcs@163.com
地址:湖南省长沙市高新技术开发区青山路699号湖南省军民融合科技创新产业园8栋B座1609室
微信公众号
Copyright © 康森特生物科技(长沙)有限公司 2024
本网站销售的所有产品均不得用于人类或动物之临床诊断或治疗,仅可用于工业或者科研等非医疗目的。

售前:+86-0731-84228665
+86 -180 7516 6076
售后:+86 -180 7516 7741
传真:+86-0731-84228665


