新闻资讯

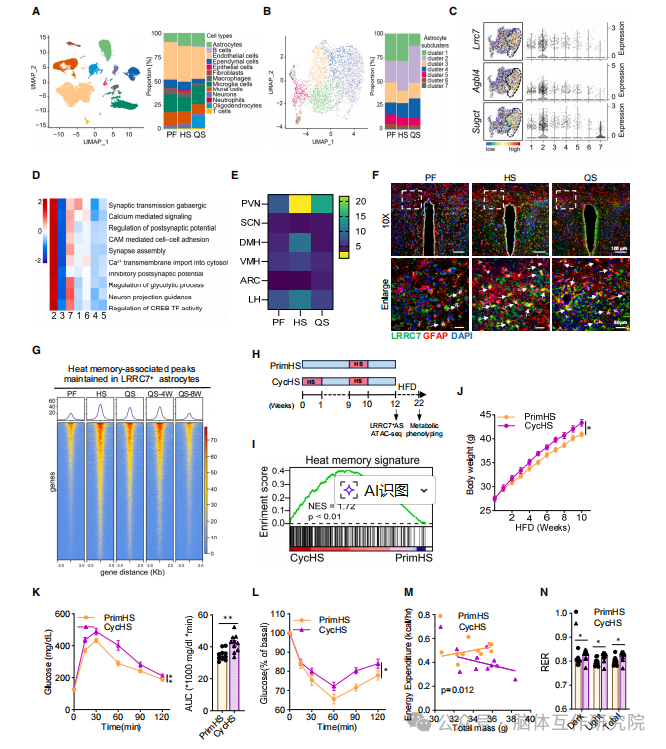
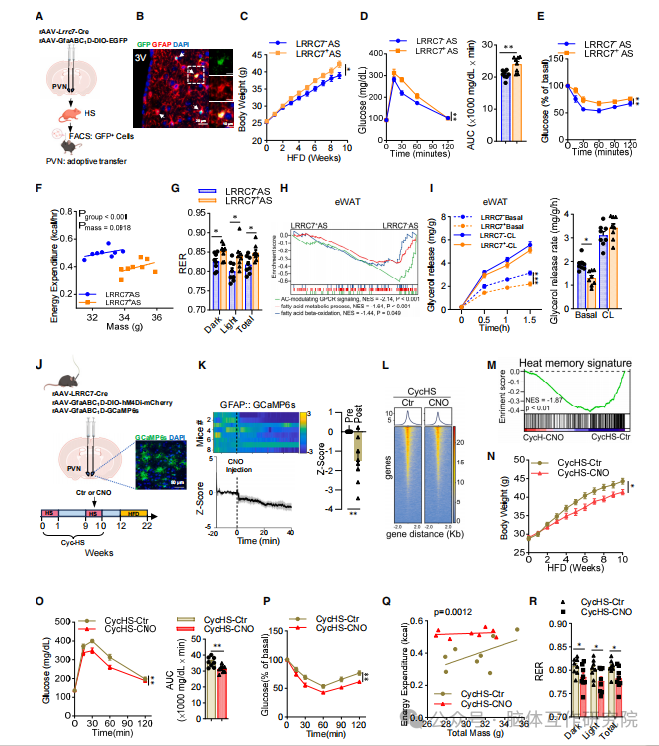
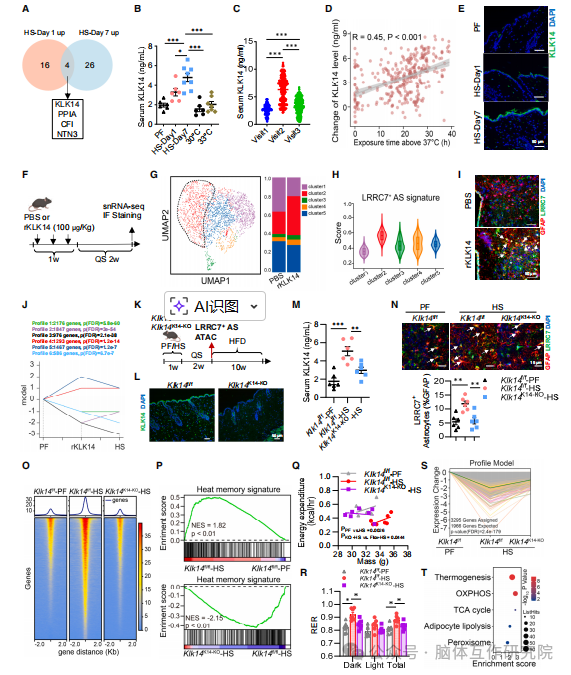
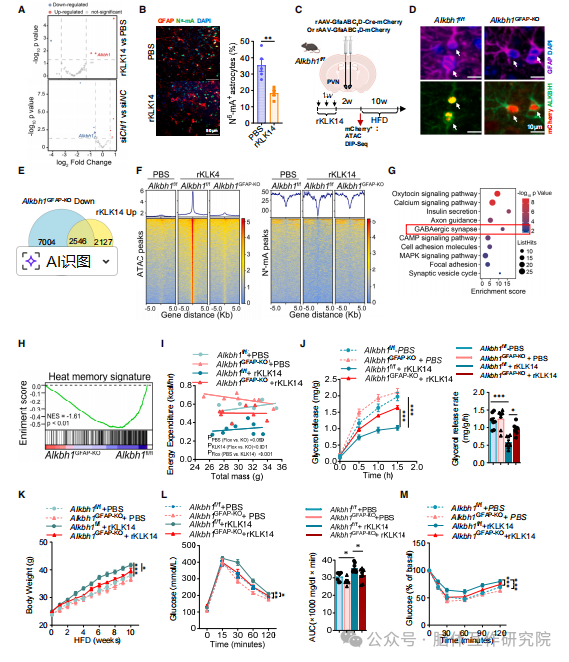
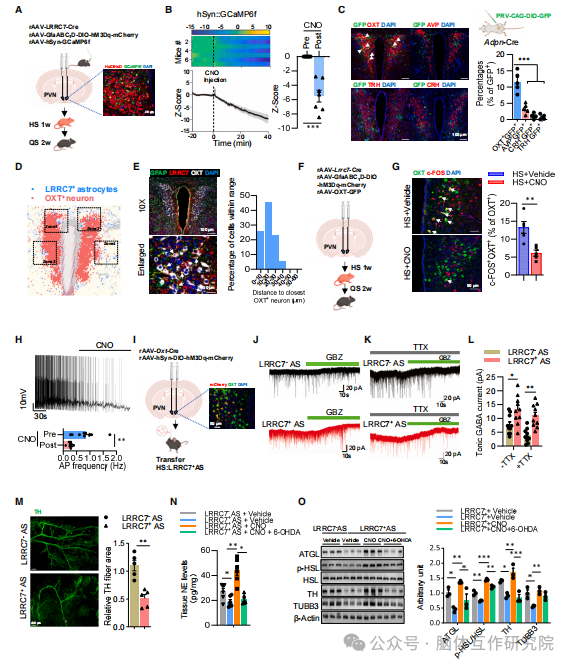
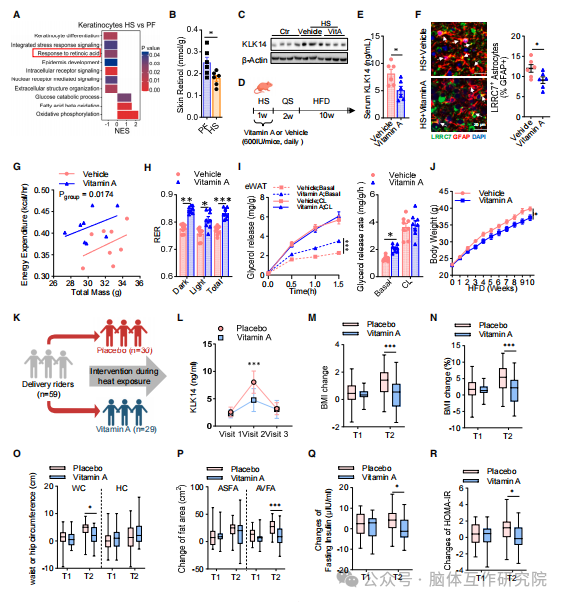
2026年4月21日,中南大学湘雅医院罗湘杭教授、黄燕教授及山东第一医科大学附属省立医院赵家军教授团队在《Cell》上发表了一篇名为“A skin-hypothalamus axis couples heat stress and metabolic dysfunction”的文章。研究旨在明确长期热应激对机体代谢健康的持续性影响,系统揭示热暴露与代谢功能障碍之间的内在关联;深入探索热应激诱发代谢异常的分子与细胞机制,精准定位参与该过程调控的关键细胞类型、信号分子及信号通路;进一步解析皮肤 - 下丘脑轴在热应激介导代谢紊乱中的核心调控作用,阐明皮肤来源信号调控中枢神经、进而影响全身代谢稳态的作用模式;在此基础上筛选可有效逆转热应激所致代谢损伤的潜在干预靶点,重点验证维生素 A 对热相关代谢异常的改善效果,为全球变暖背景下代谢相关疾病的防控提供新策略;同时将动物实验结论进行人群层面验证,评估研究结果在人类群体中的适用性,为临床预防与治疗热暴露相关代谢疾病夯实理论基础与科学依据。 01 研究方法 2.1 动物模型构建 研究首先建立小鼠热应激模型,设立室温对照组、配对喂养组与热应激组,严格管控热暴露条件及恢复周期,并分别采用普通饲料与高脂饲料进行处理干预。同时构建皮肤特异性 KLK14 敲除小鼠、星形胶质细胞特异性 ALKBH1 敲除小鼠及 CHL1 敲低小鼠等多种基因编辑动物模型,实现关键基因的组织特异性调控。研究借助病毒介导的基因操控手段,于小鼠下丘脑室旁核注射 AAV 病毒,完成对 LRRC7⁺星形胶质细胞的特异性标记、激活与抑制;此外通过细胞移植实验,将分离纯化的 LRRC7⁺与 LRRC7⁻星形胶质细胞定点移植至小鼠下丘脑,对比观察不同细胞处理后机体代谢表型的差异改变。 2.2 临床人群研究 依托前瞻性队列研究体系,以夏季长期处于高温暴露环境的长沙外卖骑手为研究人群,持续监测受试者高温暴露特征,并通过多时点随访追踪评估机体各项代谢指标的动态变化。同时开展随机双盲安慰剂对照临床试验,将研究人群随机分为维生素 A 干预组与安慰剂对照组,从临床层面验证维生素 A 补充干预对热应激相关代谢异常的改善作用与应用潜力。 2.3 分子与细胞实验 综合运用单细胞测序、单细胞核测序及空间转录组技术,系统解析下丘脑各细胞亚群的分子表达特征与空间分布规律。借助 ATAC-seq、DIP-seq 等表观遗传检测技术,探究热应激刺激下染色质开放程度及 DNA 甲基化修饰的动态改变。通过免疫共沉淀、分子对接、pull-down 联合质谱分析等实验,筛选并验证皮肤分泌蛋白 KLK14 的作用受体 CHL1。利用电生理记录、活体钙成像技术,实时监测神经元与星形胶质细胞的活性波动;结合免疫荧光、蛋白免疫印迹、ELISA 等常规分子生物学技术,定量检测组织内目标蛋白表达水平与外周血清关键因子含量。 2.4 代谢表型检测 系统检测小鼠体重、空腹血糖、糖耐量及胰岛素敏感性等核心基础代谢指标。利用全自动代谢笼系统,动态监测动物能量消耗、呼吸交换率、自主活动量等整体能量代谢相关参数。同时检测小鼠脂肪组织重量、脂肪脂解能力及组织交感神经支配水平,全面评估热应激状态下机体脂肪代谢功能的异常改变。 02 研究内容 3.1 热应激加速小鼠与人类代谢功能障碍 经历热应激处理的小鼠,在恢复期给予高脂饮食干预后,会出现体重异常增长、糖耐量受损及胰岛素抵抗等一系列代谢紊乱特征,同时伴随明显的内脏脂肪蓄积。在机制层面,热应激能够抑制脂肪组织脂解过程与脂肪酸氧化通路,造成机体能量消耗下降、脂肪供能比例降低,而交感神经调控作用减弱是该过程的关键诱因。临床队列研究结果表明,外卖骑手长期高温暴露状态,与体重、体质量指数、腹型肥胖及胰岛素抵抗相关指标的持续升高密切相关,极端高温环境带来的不良影响更为突出。综上,热应激可在机体中形成长期代谢记忆,提升高脂饮食诱导代谢紊乱的易感程度,这一病理特征在小鼠模型与人类群体中均得到验证。 图1. 高浓度(HS)暴露会加速小鼠和人类的代谢功能障碍 3.2 下丘脑 LRRC7⁺星形胶质细胞储存热应激记忆 单细胞测序结果证实,热应激刺激会促使小鼠下丘脑星形胶质细胞整体数量增多,其中 LRRC7⁺星形胶质细胞亚群发生特异性扩增,即便进入恢复阶段,该细胞亚群仍可维持较高占比。LRRC7⁺星形胶质细胞主要富集分布于下丘脑室旁核,是下丘脑内响应热应激刺激的核心细胞类群。表观遗传测序分析显示,热应激可诱导 LRRC7⁺星形胶质细胞产生持续性染色质开放重塑,进而形成稳定的热应激记忆,该表观遗传改变可维持四周以上,且二次热暴露能够快速重新激活该记忆状态。具备热应激记忆的机体再次接受高温刺激后,代谢紊乱症状会进一步加剧,充分说明 LRRC7⁺星形胶质细胞介导的热记忆是诱发代谢功能异常的重要因素。 图2. 下丘脑LRRC7+星形胶质细胞在热应激(HS)后仍保留持续的热记忆 3.3 LRRC7⁺星形胶质细胞热记忆诱发代谢紊乱 研究通过病毒标记与细胞分选手段,高效分离并纯化 LRRC7⁺与 LRRC7⁻两种星形胶质细胞亚型。将携带热记忆的 LRRC7⁺星形胶质细胞移植至正常小鼠下丘脑后,实验小鼠在高脂饮食条件下会出现肥胖、胰岛素抵抗、能量代谢水平降低等典型异常表型,与热应激模型小鼠的生理特征高度吻合。利用化学遗传学技术特异性抑制 LRRC7⁺星形胶质细胞活性,能够有效清除细胞热记忆,显著缓解热应激引发的代谢紊乱,恢复机体能量消耗水平与脂肪脂解功能。以上研究充分证实,LRRC7⁺星形胶质细胞所形成的热应激记忆,是介导热应激相关代谢失衡的核心细胞机制。 图3. LRRC7+星形胶质细胞的热记忆使小鼠易发生饮食诱导的代谢功能障碍 3.4 皮肤来源 KLK14 印记 LRRC7⁺星形胶质细胞 热应激状态下小鼠血清内 KLK14 蛋白表达水平显著上调,该分泌蛋白能够穿透血脑屏障靶向作用于下丘脑组织,进而诱导 LRRC7⁺星形胶质细胞发生特异性扩增。皮肤表皮角质形成细胞是热应激条件下循环 KLK14 的主要分泌来源,高温刺激可显著激活角质形成细胞合成与释放 KLK14。人群临床研究同样发现,高温暴露会导致外卖骑手血清 KLK14 含量上升,且蛋白水平与高温暴露时长呈正向关联。皮肤特异性敲除 KLK14 基因,可有效阻断热应激诱导的 LRRC7⁺星形胶质细胞增殖与热记忆形成,全面逆转后续代谢紊乱表型。机制探究进一步筛选并验证,CHL1 是 LRRC7⁺星形胶质细胞表面介导 KLK14 作用的功能性受体,抑制 CHL1 表达可有效阻断 KLK14 介导的代谢损伤效应。 图4. LRRC7+星形胶质细胞在HS条件下受到皮肤来源KLK14的印记调控 3.5 ALKBH1 调控 KLK14 诱导的表观遗传热记忆 KLK14 与细胞膜表面受体 CHL1 结合后,可通过下游信号通路上调 LRRC7⁺星形胶质细胞内 ALKBH1 的表达水平。ALKBH1 能够通过去除 DNA N⁶-mA 甲基化修饰,调控染色质开放状态,稳定细胞的热应激表观遗传记忆。星形胶质细胞特异性敲除 ALKBH1,可显著抑制 KLK14 诱导的染色质结构重塑,阻碍热记忆的建立与维持,有效恢复机体能量代谢稳态与脂肪脂解能力。该部分研究明确了 ALKBH1 介导的表观遗传修饰调控,是衔接皮肤来源 KLK14 信号与星形胶质细胞功能重塑、推动热记忆形成的核心分子机制。 图5. ALKBH1调控KLK14诱导的LRRC7+星形胶质细胞表观遗传记忆 3.6 LRRC7⁺星形胶质细胞抑制 PVN⁰ˣᵗ神经元 - SNS 通路 LRRC7⁺星形胶质细胞可通过合成并释放抑制性神经递质 GABA,选择性下调下丘脑室旁核催产素神经元的电活动与生理功能。神经环路示踪结果证实,下丘脑室旁核催产素神经元能够通过交感神经系统,远距离支配内脏脂肪组织,精准调控脂肪脂解代谢进程。LRRC7⁺星形胶质细胞对催产素神经元的持续抑制作用,会减弱脂肪组织交感神经支配强度,降低局部去甲肾上腺素分泌水平,最终抑制脂肪分解代谢,促进内脏脂肪异常堆积。特异性激活下丘脑室旁核催产素神经元,可有效逆转 LRRC7⁺星形胶质细胞异常活化引发的代谢障碍,证实该神经环路是热应激扰乱代谢稳态的关键调控通路。 图6.LRRC7阳性星形胶质细胞抑制 PVNOXT 神经元-交感神经系统(SNS)回路,从而抑制内脏脂肪沉积。 3.7 维生素 A 改善热应激诱导的代谢紊乱 长期热应激干预会造成皮肤组织内维生素 A 含量下降,补充维生素 A 可有效抑制热应激下角质形成细胞中 KLK14 的合成与分泌。动物实验结果表明,外源性补充维生素 A 能够降低小鼠血清 KLK14 浓度,减少下丘脑 LRRC7⁺星形胶质细胞异常增殖,恢复机体能量消耗与脂肪脂解功能,全面改善热应激诱发的各类代谢异常。依托临床随机干预试验进一步验证,维生素 A 补充可有效降低高温暴露人群血清 KLK14 水平,缓解体重增加、腹围增大、内脏脂肪堆积及胰岛素抵抗等不良代谢改变,且全程干预安全性良好,为热暴露相关代谢疾病的预防与干预提供了安全可行的靶向策略。 图7. 维生素A可改善高硫暴露小鼠和人类的KLK14水平,并缓解代谢功能障碍 03 创新点 首次发现皮肤 - 下丘脑调控轴:揭示皮肤在热应激下分泌 KLK14,作用于下丘脑 LRRC7⁺星形胶质细胞,建立跨器官的热应激感知与代谢调控新通路。 鉴定 LRRC7⁺星形胶质细胞为热记忆载体:发现下丘脑特异性星形胶质细胞亚群可通过表观遗传修饰储存热记忆,是连接环境热暴露与长期代谢异常的核心细胞靶点。 解析完整分子调控链条:构建 “热应激→皮肤 KLK14→星形胶质细胞 CHL1→ALKBH1 表观修饰→GABA 抑制 PVN⁰ˣᵗ神经元→交感神经减弱→脂肪堆积” 的完整机制。 04 启发 5.1 科研思路启发 全球变暖等环境变化已成为代谢性疾病发生发展的重要诱因,聚焦环境应激与慢性疾病的内在联系,从环境暴露角度深入解析代谢紊乱的潜在机制,可为慢病研究开辟全新的科研方向。同时需重视器官间交叉通讯的调控作用,皮肤作为人体最大的外周器官,能够通过分泌功能性信号分子远距离调控中枢神经系统生理功能,为神经 - 内分泌 - 免疫调控网络的机制探索提供崭新研究视角。环境刺激可通过诱导表观遗传修饰重塑,在细胞与机体层面留存长期功能性记忆,表观遗传记忆也是介导环境应激持续损伤的关键调控模式,靶向干预表观遗传调控通路,有望成为防治环境相关性疾病的有效策略。此外,基础研究应持续立足临床需求,推动动物模型中的机制发现向人群研究延伸,结合临床试验开展功效验证,高效打通基础研究与临床转化通路,充分释放科研成果的实际应用价值。 5.2 实际应用启发 长期高温暴露会显著提升肥胖、胰岛素抵抗及糖尿病等代谢问题的发病风险,因此需重点关注高温作业特殊人群的健康管理,强化该群体代谢指标的常态化监测,落实早期筛查与针对性干预防护。维生素 A 可有效缓解热应激引发的代谢损伤,通过日常科学合理补充,能够减轻高温暴露带来的代谢异常损害,为热相关代谢损伤提供安全可行的防护方案。以 KLK14、ALKBH1、CHL1 等核心调控分子为靶点,可进一步研发新型靶向药物,为肥胖、胰岛素抵抗等代谢性疾病的临床治疗提供全新作用靶点与研发方向。在公共卫生领域,需充分重视全球变暖背景下持续性高温环境对全民代谢健康的潜在危害,结合环境变化与人群健康数据,制定科学完善的公共健康防护策略与干预政策,全面提升人群环境适应性健康保障能力。 参考文献: Zhou HY, Feng X, Wen J, Xiao Y, Wang LW, Chen LY, Xie GQ, Zhao JJ, Huang Y, Luo XH. A skin-hypothalamus axis couples heat stress and metabolic dysfunction. Cell. 2026 Apr 21:S0092-8674(26)00346-6. doi: 10.1016/j.cell.2026.03.045IF: 42.5 Q1 . Epub ahead of print. PMID: 42019490.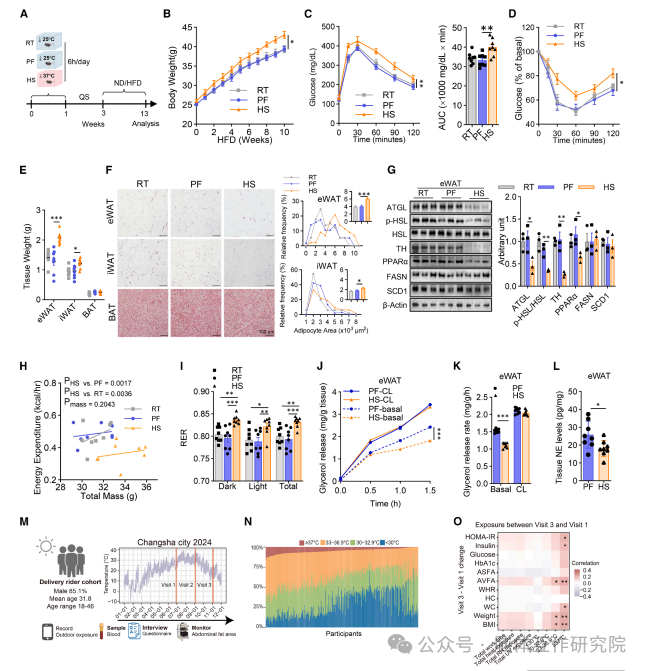
厚谱实验室(脑体互作研究—神经药效评价实验室0专注于脑体互作机制解析与神经药效精准评价的尖端实验技术高地。可以开展清醒动物小分子取样分析、神经递质代谢产物实时分析、癫痫睡眠脑电采集分析、在体电生理记录分析、脑机接口方案评价(大动物脑部手术)、神经调控、组织透明化、脊髓损伤康复验证实验电生理(SEP)、脑立体定位给药、自动无接触采血分析、葡萄糖钳夹实验、行为学迷宫实验和动物造模等各种动物实验服务!
-END-
想了解更多内容,获取相关咨询请联系 电 话:+86-0731-84428665 伍经理:+86-180 7516 6076 工程师:+86-180 7311 8029 邮 箱:consentcs@163.com


订购和售后

邮箱:consentcs@163.com
地址:湖南省长沙市高新技术开发区青山路699号湖南省军民融合科技创新产业园8栋B座1609室
微信公众号
Copyright © 康森特生物科技(长沙)有限公司 2024
本网站销售的所有产品均不得用于人类或动物之临床诊断或治疗,仅可用于工业或者科研等非医疗目的。

售前:+86-0731-84228665
+86 -180 7516 6076
售后:+86 -180 7516 7741
传真:+86-0731-84228665


